 Человек на восемьдесят процентов состоит из воды. Поэтому качество питьевой воды чрезвычайно важно для нормального существования как человека, так и всех живых существ. Качество питьевой воды на сегодняшний день – это пока еще открытый вопрос. Что именно должно содержаться в этой жидкости и можно ли достать ее где-либо обычному гражданину?
Человек на восемьдесят процентов состоит из воды. Поэтому качество питьевой воды чрезвычайно важно для нормального существования как человека, так и всех живых существ. Качество питьевой воды на сегодняшний день – это пока еще открытый вопрос. Что именно должно содержаться в этой жидкости и можно ли достать ее где-либо обычному гражданину?
Может быть, такую жидкость можно обнаружить лишь в горных реках или глубинных скважинах? Конечно же, лучше всего употреблять воду, которая минимально подвергается человеческому воздействию. Ведь жидкость эта снимает всю информацию со всего, с чем соприкасается. Потом эта информация поступает в организм. Оттуда и масса заболеваний. Какую питьевую воду мы пили множество десятилетий назад? Прошедшую промышленную очистку, множество ступеней и фильтров, а в конечном итоге хлорированную. Как она попадала к нам на стол? Через ржавые и покрытые слизью трубы, не меняющиеся десятилетиями. Может ли подобный напиток нести хорошую энергетику? А сколько вредных примесей в этой жидкости? Сегодня есть масса выходов для людей, заботящихся о своем здоровье и ведущих здоровый образ жизни. Можно приобретать очищенную воду в бутылках. Производителей этого товара масса. Среди этого разнообразия можно выбрать производителя, достойного доверия и использовать только его продукцию. Можно приобрести фильтр для воды домашнего применения. Тогда следует внимательно следить за сроками действия картриджей. Иначе целебная влага со временем станет концентратом всех вредных примесей, осевших в фильтрах.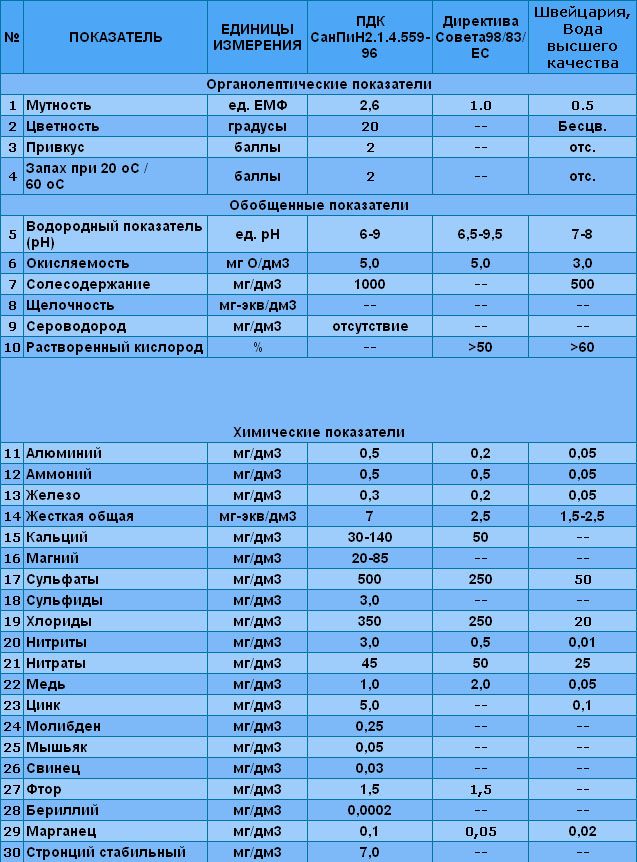
Существуют основные показатели качества питьевой воды. Их условно можно разделить на группы:
Органолептические показатели (запах, привкус, цветность, мутность)
Токсикологические показатели (алюминий, свинец, мышьяк, фенолы, пестициды)
Показатели, влияющие на органолептические свойства воды (рН, жесткость общая, нефтепродукты, железо, марганец, нитраты, кальций, магний, окисляемость перманганатная, сульфиды)
Химические вещества, образующиеся при обработке воды (хлор остаточный свободный, хлороформ, серебро)
Микробиологические показатели (термотолерантные колиформы или Е. соli, ОМЧ).
Опыт работы лаборатории по анализу качества воды показал, что к наиболее распространенным загрязнителям воды (содержание компонентов превышает нормативы), скажем в Московской обл., можно отнести железо, марганец, сульфиды, фториды, соли кальция и магния, органические соединения и другие вещества.
Описание свойств и химических элементов воды
|
Температура воды |
поверхностных источников зависит от температуры воздуха, его влажности, скорости и характера движения воды и ряда других факторов. Она может изменяться в значительных пределах. Температура воды подземных источников относительно постоянна и составляет обычно 4-8 оС. Оптимальной температурой воды для питьевых целей считается 7-11 оС. |
|
Цветность воды |
(интенсивность окраски) выражается в градусах по платиново-кобальтовой шкале. Один градус шкалы соответствует цвету 1 литра воды, окрашенного добавлением 1 мг соли - хлорплатината кобальта. Цветность воды подземных вод вызывается соединениями железа, реже - гумусовыми веществами (грунтовка, торфяники, мерзлотные воды); цветность поверхностных - цветением водоемов. По нормам СанПиН 2.1.4.1074-01 на питьевую воду, цветность воды не должна быть выше 20 град. (в особых случаях не выше 35 град.) Многие виды промышленности предъявляют гораздо более жесткие требования в отношении цветности используемой воды. |
|
Мутность |
(прозрачность, содержание взвешенных веществ) характеризует наличие в воде частиц песка, глины, илистых частиц, планктона, водорослей и других механических примесей, которые попадают в нее в результате размыва дна и берегов реки, с дождевыми и талами водами, со сточными водами и т.п. Мутность воды подземных источников, как правило, невелика и обуславливается взвесью гидрооксида железа. В поверхностных водах мутность чаще обусловлена присутствием фито- и зоопланктона, глинистых или илистых частиц, поэтому величина зависит от времени паводка (межени) и меняется в течении года. По нормам СанПиН 2.1.4.1074-01 мутность питьевой воды должна быть не выше 1,5 мг/л. На многих производствах можно использовать воду с гораздо большим содержанием взвешенных веществ, чем определено ГОСТом. В то же время для некоторых производств химической, пищевой, электронной, медицинской и других видов промышленности требуется вода такого же или даже более высокого качества. |
|
Вкус |
вызывается наличием в воде растворенных веществ и может быть соленым, горьким, сладким и кислым. Природные воды обладают, как правило, только солоноватым и горьковатым привкусом. Солёный вкус вызывается содержанием хлорида натрия, горький - сульфата магния. Кислый вкус воде придаёт большое количество растворённой углекислоты. Вода может иметь также чернильный или железистый привкус, вызванный солями железа и марганца или вяжущий привкус, вызванный сульфатом кальция. По нормам СанПиН 2.1.4.559-96, привкус должен быть не более 2 баллов. |
|
Запахи |
воды определяются живущими и отмершими организмами, растительными остатками, специфическими веществами, выделяемыми некоторыми водорослями и микроорганизмами, а также присутствием в воде растворенных газов - хлора, аммиака, сероводорода, меркаптанов или органических и хлорорганических загрязнений. Различают природный запахи: ароматический, болотный, гнилостный, древесный, землистый, плесневый, рыбный, травянистый, неопределённый и сероводородный. Запахи искусственного происхождения называют по определяющим их веществам: фенольный, хлорфенольный, нефтяной, смолистый и так далее. Интенсивность запаха измеряется органолептически по пятибалльной шкале: |
|
Содержание растворенных веществ (сухой остаток) |
Общее количество веществ (кроме газов), содержащихся в воде в растворенном состоянии, характеризуется сухим остатком, получаемых в результате выпаривания профильтрованной воды и высушивания задержанного остатка до постоянной массы. В воде, используемой для хозяйственно-питьевых целей, сухой остаток не должен превышать 1000 мг/л в особых случаях - 1500 мг/л. Общее солесодержание и сухой остаток характеризуют минерализацию (содержание растворенных солей в воде). По СанПиН 2.1.4.1074-01 на питьевую воду, сухой остаток должен быть не более 1000 мг/л |
|
Активная реакция воды |
степень её кислотности или щёлочности - определяется концентрацией водородных ионов. Обычно выражается через рН - отрицательный логарифм концентрации ионов водорода. При рН = 7,0 реакция воды нейтральная, при рН < 7,0 среда кислая, при рН > 7,0 среда щелочная. По нормам СанПиН 2.1.4.559-96 рН питьевой воды должен быть в пределах 6,0…9,0 Для вод большинства природных источников значение рН не отклоняется от указанных пределов. Однако после обработки вод реагентами значение рН может существенно измениться. Для правильной оценки качества воды и выбора способа очитски необходимо знать значение рН воды источника в различные периоды года. При низких значениях сильно возрастает ее коррозирующее действие на сталь и бетон. Очень часто для описания качества воды используется термин - жесткость. Пожалуй, самое большое расхождение между российскими нормами и директивой Совета ЕС по качеству воды относится к жесткости: 7 мг-экв/л у нас и 1 мг-экв/л у них. Жесткость самая наиболее распространенная проблема качества воды. |
|
Жесткость |
воды определяется содержанием в воде солей жесткости (кальция и магния). Она выражается в миллиграмм-эквивалентах на литр (мг-экв/л). Различают следующие виды жесткости: Общая - сумма карбонатной и некарбонатной жесткости. Вода поверхностных источников, как правило, относительно мягкая (3…6 мг-экв/л) и зависит от географического положения - чем южнее, тем жесткость воды выше. Жесткость подземных вод зависит от глубины и расположения горизонта водоносного слоя и годового объема осадков. Жесткость воды из слоёв известняка составляет обычно 6 мг-экв/л и выше. По нормам СанПиН 2.1.4.1074-01 жесткость питьевой воды должна быть не выше 7 (10) мг-экв/л, ( или не более 350 мг/л). очень мягкая вода до 1,5 мг-экв/л мягкая вода от 1,5 до 4 мг-экв/л вода средней жесткости от 4 до 8 мг-экв/л жесткая вода от 8 до 12 мг-экв/л очень жесткая вода более 12 мг-экв/л Жесткая вода просто неприятна на вкус, в ней излишне много кальция. Постоянное употребление внутрь воды с повышенной жесткостью приводит к снижению моторики желудка, к накоплению солей в организме, и, в конечном итоге, к заболеванию суставов (артриты, полиартриты) и образованию камней в почках и желчных путях. Хотя очень мягкая вода не менее опасная, чем излишне жесткая. Самая активная - это мягкая вода. Мягкая вода способна вымывать из костей кальций. У человека может развиться рахит, если пить такую воду с детства, у взрослого человека становятся ломкие кости. Есть еще одно отрицательное свойство мягкой воды. Она, проходя через пищеварительный тракт, не только вымывает минеральные вещества, но и полезные органические вещества, в том числе и полезные бактерии. Вода должна быть жесткостью не менее 1,5-2 мг-экв/л. Использование воды с большой жесткостью для хозяйственных целей также нежелательно. Жесткая вода образует налет на сантехнических приборах и арматуре, образует накипные отложения в водонагревательных системах и приборах. В первом приближении это заметно на стенках, например, чайника. При хозяйственно-бытовом использовании жесткой воды значительно увеличивается расход моющих средств и мыла вследствие образования осадка кальциевых и магниевых солей жирных кислот, замедляется процесс приготовления пищи (мяса, овощей и др.), что нежелательно в пищевой промышленности. Во многих случаях использование жесткой воды для производственных целей (для питания паровых котлов, в текстильной бумажной промышленности, на предприятиях искусственного волокна и др.) не допускается, так как это связано с рядом нежелательных последствий. В системах водоснабжения - жесткая вода приводит к быстрому износу водонагревательной технике (бойлеров, батарей центрального водоснабжения и др.). Соли жесткости (гидрокарбонаты Ca и Mg), отлагаясь на внутренних стенках труб, и образуя накипные отложения в водонагревательных и охлаждающих системах, приводят к занижению проходного сечения, уменьшают теплоотдачу. Не допускается использовать воду с высокой карбонатной жесткостью в системах оборотного водоснабжения. Содержание сульфатов и хлоридов. Сульфаты и хлориды кальция и магния образуют соли некарбонатной жесткости. |
|
Щёлочность воды |
Под общей щёлочностью воды подразумевается сумма содержащихся в ней гидратов и анионов слабых кислот (угольной, кремниевой, фосфорной и т.д.). В подавляющем большинстве случаев для подземных вод имеется в виду гидрокарбонатная щёлочность, то есть содержание в воде гидрокарбонатов. ПДК по щелочности составляет 0,5 - 6,5 ммоль / дм3 |
|
Хлориды |
присутствуют практически во всех водах. В основном их присутствие в воде связано с вымыванием из горных пород наиболее распространённой на Земле соли - хлорида натрия (поваренной соли). Хлориды натрия содержатся в значительных количествах в воде морей, а также некоторых озер и подземных источников ПДК хлоридов в воде питьевого качества - 300...350 мг/л (в зависимости от стандарта). Повышенное содержание хлоридов в совокупности с присутствием в воде аммиака, нитритов и нитратов может свидетельствовать о загрязнённости бытовыми сточными водами. |
|
Сульфаты |
попадают в подземные воды в основном при растворении гипса, находящегося в пластах. Повышенное содержание сульфатов в воде приводит к расстройству желудка (тривиальные названия сульфата магния и сульфата натрия (солей, обладающих слабящим эффектом) - "английская соль" и "глауберова соль" соответственно). ПДК сульфатов в воде питьевого качества - 500 мг/л. |
|
Содержание кремниевых кислот |
Кремниевые кислоты встречаются в воде как подземных, так и поверхностных источников в различной форме (от коллоидной до ионодисперсной). Кремний отличается малой растворимостью и его в воде, как правило, не много. Попадает кремний в воду и с промышленными стоками предприятий, производящих керамику, цемент, стекольные изделия, силикатные краски. ПДК кремния - 10 мг/л. Воды, содержащие кремниевые кислоты, не могут быть использованы для питания котлов высокого давления, так как образуют силикатную накипь на стенках. |
|
Фосфаты |
обычно присутствуют в воде в небольшом количестве, поэтому их присутствие указывает на возможность загрязнения промышленными стоками или стоками с сельскохозяйственных полей. Повышенное содержание фосфатов оказывает сильное влияние на развитие сине-зелёных водорослей, выделяющих токсины в воду при отмирании. ПДК в питьевой воде соединений фосфора составляет 3,5 мг/л. |
|
Фториды и йодиды |
Фториды и йодиды в чём-то похожи. Оба элемента при недостатке или избытке в организме приводят к серьёзным заболеваниям. Для йода это - заболевания щитовидной железы ("зоб"), возникающие при суточном рационе менее 0,003 мг или более 0,01 мг. Для восполнения дефицита йода в организме возможно употребление йодированной соли, но лучший выход - это включение в рацион рыбы и морепродуктов. Особенно богата йодом морская капуста. Фториды входят в состав минералов - солей фтора. Как недостаток, так и избыток фтора могут приводить к серьезным заболеваниям. Содержание фтора в питьевой должно поддерживаться в пределах 0,7 - 1,5 мг/л (в зависимости от климатических условий) Воды поверхностных источников характеризуются преимущественно низким содержанием фтора (0,3-0,4 мг/л). Высокие содержания фтора в поверхностных водах являются следствием сброса промышленных фторсодержащих сточных вод или контакта вод с почвами, богатыми соединениями фтора. Максимальные концентрации фтора (5-27 мг/л и более) определяют в артезианских и минеральных водах, контактирующих с фторсодержащими водовмещающими породами. При гигиенической оценке поступления фтора в организм важное значение имеет содержание микроэлемента в суточном рационе, а не в отдельных пищевых продуктах. В суточном рационе содержится от 0,54 до 1,6 мг фтора (в среднем 0,81 мг). Как правило, с пищевыми продуктами в организм человека поступает в 4-6 раз меньше фтора, чем при употреблении питьевой воды, содержащей оптимальные его количества (1 мг/л). Повышенное содержание фтора в воде (более 1,5 мг/л) оказывает вредное влияние на людей и животных, у населения развивается эндемический флюороз ("пятнистая эмаль зубов"), рахит и малокровие. Отмечается характерное поражение зубов, нарушение процессов окостенения скелета, истощение организма. Содержание фтора в питьевой воде лимитируется. Установлено, что систематическое использование населением фторированной воды снижает и уровень заболеваний, связанных с последствиями одонтогенной инфекции (ревматизм, сердечно-сосудистая патология, заболевания почек и др.). Недостаток фтора в воде (менее 0,5 мг/л) приводит к кариесу. При пониженном содержание фтора в питьевой воде рекомендуется пользоваться зубной пастой с добавлением фтора. Фтор - один из немногих элементов, которые лучше усваиваются организмом из воды. Оптимальная доза фтора в питьевой воде составляет 0,7...1,2 мг/л. ПДК фтора составляет 1,5 мг/л. |
|
Окисляемость |
обусловлена содержанием в воде органических веществ и отчасти может служить индикатором загрязнённости источника сточными водами. Различают окисляемость перманганатную и окисляемость бихроматную (или ХПК - химическая потребность в кислороде). Перманганатная окисляемость характеризует содержание легкоокисляемой органики, бихроматная - общее содержание органических веществ в воде. По количественному значению показателей и их отношению можно косвенно судить о природе органических веществ, присутствующих в воде, о пути и эффективности технологии очистки. По нормам СанПиН перманганатная окисляемость воды должна быть не выше 5,0 мг О2/л и предельно допустимая концентрация (ПДК) 2 мг-экв/л. Если меньше 5 мг-экв/л вода считается чистой, больше 5 грязной. |
|
Содержание соединений железа |
Железо может встречаться в природных водах в следующих видах: - Истинно растворённом виде (двухвалентное железо, прозрачная бесцветная вода); В поверхностных водах средней полосы России содержится от 0,1 до 1 мг/дм3 железа, в подземных водах содержание железа часто превышает 15-20 мг/дм3. Значительные количества железа поступают в водоемы со сточными водами предприятий металлургической, металлообрабатывающей, текстильной, лакокрасочной промышленности и с сельскохозяйственными стоками. Очень важен анализ на содержание железа для сточных вод. Концентрация железа в воде зависит от рН и содержания кислорода в воде. Железо в воде колодцев и скважин может находится как в окисленной, так и в востановленной форме, но при отстаивании воды всегда окисляется и может выпадать в осадок. Много железа растворено в кислых бескислородных подземных водах. По нормам СанПиН 2.1.4.1074-01 содержание железа общего допускается не более 0,3 мг/л. Длительное употребление человеком воды с повышенным содержанием железа может привести к заболеванию печени (гемосидерит), увеличивает риск инфарктов, негативно влияет на репродуктивную функцию организма. Такая вода неприятна на вкус, причиняет неудобства в быту. На многих промышленных предприятиях, где вода употребляется для промывки продукта в процессе его изготовления, в частности в текстильной промышленности, даже невысокое содержание железа в воде приводит к браку продукции. |
|
Марганец |
встречается в аналогичных модификациях. Марганец активизирует ряд ферментов, участвует в процессах дыхания, фотосинтеза, влияет на кроветворение и минеральный обмен. Недостаток марганца в почве вызывает у растений некрозы, хлорозы, пятнистости. При недостатке этого элемента в кормах животные отстают в росте и развитии, у них нарушается минеральный обмен, развивается анемия. На почвах, бедных марганцем (карбонатных и переизвесткованных), применяют марганцевые удобрения. Для человека опасен как недостаток, так и переизбыток марганца. По нормам СанПиН 2.1.4.1074-01 содержание марганца допускается не более 0,1 мг/л. Избыток марганца вызывает окраску и вяжущий привкус, заболевание костной системы. Присутствие в воде железа и марганца может способствовать развитию в трубах и теплообменных аппаратах железистых и марганцевых бактерии, продукты жизнедеятельности которых вызывают уменьшение сечения, а иногда их полную закупорку. Содержание железа и марганца строго ограничено в воде, используемой при производстве пластмасс, текстильной, пищевой промышленности и т.п. Повышенное содержание обоих элементов в воде вызывает потёки на сантехнике, окрашивает бельё при стирке и придаёт воде железистый или чернильный привкус. Длительное употребление такой воды для питья вызывает отложение указанных элементов в печени и по вредности значительно обгоняет алкоголизм. ПДК железа - 0,3 мг/л, марганца - 0,1 мг/л. |
|
Натрий и калий |
попадают в подземные воды за счёт растворения коренных пород. Основным источником натрия в природных водах являются залежи поваренной соли NaCl, образовавшиеся на месте древних морей. Калий встречается в водах реже, так как он лучше поглощается почвой и извлекается растениями. Биологическая роль натрия крайне важна для большинства форм жизни на Земле, включая человека. Организм человека содержит около 100 г натрия. Ионы натрия активируют ферментативный обмен в организме человека. ПДК натрия составляет 200 мг/л. Избыточное содержание натрия в воде и пище приводит к гипертензии и гипертонии. Отличительная особенность калия - его способность вызывать усиленное выведение воды из организма. Поэтому пищевые рационы с повышенным содержанием элемента облегчают функционирование сердечно-сосудистой системы при ее недостаточности, обусловливают исчезновение или существенное уменьшение отеков. Дефицит калия в организме ведет к нарушению функции нервно-мышечной (парезы и параличи) и сердечно-сосудистой систем и проявляется депрессией, дискоординацией движений, мышечной гипотонией, гипорефлек-сией, судорогами, артериальной гипотонией, брадикардией, изменениями на ЭКГ, нефритами, энтеритами и др. ПДК калия составляет 20 мг/л |
|
Медь, цинк, кадмий, свинец, мышьяк, никель, хром и ртуть |
преимущественно попадают в источники водоснабжения со стоками промышленных вод. Медь и цинк могут также попадать при коррозии соответственно оцинкованных и медных водопроводных труб из-за повышенного содержания агрессивной углекислоты. ПДК в питьевой воде согласно СанПиН меди составляет 1,0 мг/л; цинка - 5,0 мг/л; кадмия - 0,001 мг/л; свинца - 0,03 мг/л; мышьяка - 0,05 мг/л; никеля - составляет 0,1 мг/л (в странах ЕС - 0,05 мг/л), хрома Cr3+ - 0,5 мг/л, хрома Cr4+ - 0,05 мг/л; ртути - 0,0005 мг/л. Все вышеперечисленные соединения относятся к тяжёлым металлам и обладают кумулятивным действием, то есть свойством накапливаться в организме и срабатывать при превышении определённой концентрации в организме. |
|
Кадмий
|
очень токсичный металл. Избыточное поступление кадмия в организм может приводить к анемии, поражению печени, кардиопатии, эмфиземе легких, остеопорозу, деформации скелета, развитию гипертонии. Наиболее важным в кадмиозе является поражение почек, выражающееся в дисфункции почечных канальцев и клубочков с замедлением канальцевой реабсорбции, протеинурией, глюкозурией, последующими аминоацидурией, фосфатурией. Избыток кадмия вызывает и усиливает дефицит Zn и Se. Воздействие на протяжении продолжительного времени может вызывать поражение почек и легких, ослабление костей. Симптомы кадмиевого отравления: белок в моче, поражение центральной нервной системы, острые костные боли, дисфункция половых органов. Кадмий влияет на кровяное давление, может служить причиной образования камней в почках (в почках он накапливается особенно интенсивно). Опасность представляют все химические формы кадмия |
|
Алюминий |
легкий серебристо-белый металл. Попадает в воду в первую очередь в процессе водоподготовки - в составе коагулянтов и при сбросе сточных вод переработки бокситов. ПДК в воде солей алюминия составляет - 0,5 мг/л Избыток алюминия в воде приводит к повреждению центральной нервной системы. |
|
Бор и Селен |
присутствуют в некоторых природных водах в качестве микроэлементов в весьма незначительной концентрации, однако, при их превышении возможно серьёзное отравление. |
|
Содержание газов |
В воде природных источников чаще всего присутствуют следующие газы: кислород О2, диоксид углерода (углекислый газ) СО2 и сероводород Н2S |
|
Кислород |
находится в воде в растворенном виде. Растворенный кислород в подземных водах отсутствует, содержание в поверхностных водах соответствует парциальному давлению, зависит от температуры воды и интенсивности процессов, обогащающих или обедняющих воду кислородом и может достигать 14 мг/л Содержание кислорода и двуокиси углерода даже в значительных количествах не ухудшает качества питьевой воды, но способствует коррозии металла. Процесс коррозии усиливается с повышением температуры воды, а также при движении её. При значительном содержании в воде агрессивной двуокиси углерода коррозии подвергаются также стенки бетонных труб и резервуаров. В питательной воде паровых котлов среднего и высокого давления присутствие кислорода не допускается. Содержание сероводорода придает воде неприятный запах и, кроме того, вызывает коррозию металлических стенок труб, баков и котлов. В связи с этим присутствие Н2S не допускается в воде, употребляемой для хозяйственно-питьевых и для большинства производственных нужд. |
|
Вещества, содержащиеся в воде и их свойства, ухудшающие качество питьевой воды и вредно влияющие на организм человека. |
|
|
Соединения азота |
Азотосодержащие вещества (нитраты NO3-, нитриты NO2- и аммонийные соли NH4+) почти всегда присутствуют во всех водах, включая подземные, и свидетельствуют о наличии в воде органического вещества животного происхождения. Являются продуктами распада органических примесей, образуются в воде преимущественно в результате разложения мочевины и белков, поступающих в неё с бытовыми сточными водами. Рассматриваемая группа ионов находится в тесной взаимосвязи. Первым продуктом распада является аммиак (аммонийный азот) - является показателем свежего фекального загрязнения и является продуктом распада белков. В природной воде ионы аммония окисляются бактериями Nitrosomonas и Nitrobacter до нитритов и нитратов. Нитриты являются лучшим показателем свежего фекального загрязнения воды, особенно при одновременном повышенным содержании аммиака и нитритов. Нитраты служат показателем более давнего органического фекального загрязнения воды. Недопустимо содержание нитратов вместе с аммиаком и нитратами. По наличию, количеству и соотношению в воде азотсодержащих соединений можно судить о степени и давности заражения воды продуктами жизнедеятельности человека. Отсутствие в воде аммиака и в то же время наличие нитритов и особенно нитратов, т.е. соединений азотной кислоты, свидетельствуют о том, что загрязнение водоема произошло давно, и вода подверглась самоочищению. Наличие в воде аммиака и отсутствие нитратов указывают на недавнее загрязнение воды органическими веществами. Следовательно, в питьевой воде не должно быть аммиака, не допускаются соединения азотной кислоты (нитриты). По нормам СанПиН ПДК в воде аммония составляет 2,0 мг/л; нитритов - 3,0 мг/л; нитратов - 45,0 мг/л. Наличие иона аммония в концентрациях, превышающих фоновые значения, указывает на свежее загрязнение и близость источника загрязнения (коммунальные очистные сооружения, отстойники промышленных отходов, животноводческие фермы, скопления навоза, азотных удобрений, поселения и др.). Употребление воды с повышенным содержанием нитритов и нитратов приводит к нарушению окислительной функции крови. |
|
Хлор |
появляется в питьевой воде в результате её обеззараживания. Сущность обеззараживающего действия хлора заключается в окислении или хлорировании (замещении) молекул веществ, входящих в состав цитоплазмы клеток бактерий, отчего бактерии гибнут. Очень чувствительны к хлору возбудители брюшного тифа, паратифов, дизентерии, холеры. Даже сильно заражённая бактериями вода в значительной мере дезинфицируется сравнительно малыми дозами хлора. Однако отдельные хлоррезистентные особи сохраняют жизнеспособность, поэтому полной стерилизации воды не происходит. Ввиду того, что свободный хлор относится к числу вредных для здоровья веществ, гигиенические номы СанПиН строго регламентирует содержание остаточного свободного хлора в питьевой воде централизованного водоснабжения. При этом СанПиН устанавливает не только верхнюю границу допустимого содержания свободного остаточного хлора, но и минимально-допустимую границу. Дело в том, что, что несмотря на обеззараживание на станции водоочистки, готовую "товарную" питьевую воду подстерегает немало опасностей по пути к крану потребителя. Например, свищ в стальной подземной магистрали, сквозь которые не только магистральная вода попадает наружу, но и загрязнения из почвы могут попасть в магистраль. Остаточный хлор (оставшийся в воде после обеззараживания) необходим для предотвращения возможного вторичного заражения воды во время прохождения по сети. По нормам СанПиН 2.1.4.559-96 содержание остаточного хлора в водопроводной воде должно быть не менее 0,3 мг/л и не более 0,5 мг/л. Хлорированная вода неблагоприятно воздействует на кожу и слизистые оболочки, поскольку хлор является сильным аллергическим и токсическим веществом. Так, хлор вызывает покраснения различных участков кожи, а также становится причиной аллергического конъюктевита, первыми признаками которого являются жжение, слезотечение, отек век и другие болевые ощущения в области глаз. Дыхательная система также подвергается вредному воздействию: у 60% пловцов регистрируется проявление бронхоспазма после нескольких минут нахождения в бассейне с хлорированной водой. Исследования показали, что около 10% хлора, используемого при хлорировании, участвует в образовании хлорсодержащих соединений. Приоритетными хлорсодержащими соединениями являются хлороформ, четырёххлористый углерод, дихлорэтан, трихлорэтан, тетрахлоэтилен. В сумме образующихся при водоподготовке ТГМ хлороформ составляет 70 - 90 %. Хлороформ вызывает профессиональные хронические отравления с преимущественным поражением печени и центральной нервной системы. При хлорировании есть вероятность образования чрезвычайно токсичных соединений, тоже содержащих хлор, - диоксинов (диоксин в 68 тыс. раз ядовитее цианистого калия). Хлорированная вода обладает высокой степенью токсичности и суммарной мутагенной активностью (СМА) химических загрязнений, что многократно увеличивает риск онкологических заболеваний. По оценке американских экспертов, хлорсодержащие вещества в питьевой воде косвенно или непосредственно виновны в 20 онкозаболеваниях на 1 млн. жителей. Риск онкозаболеваний в России при максимальном хлорировании воды достигает 470 случаев на 1 млн. жителей. Предполагается, что 20-35% случаев заболевания раком (преимущественно толстой кишки и мочевого пузыря) обусловлены потреблением питьевой воды. |
|
Сероводород |
встречающийся в подземных водах, преимущественно неорганического происхождения. Он образуется в результате разложения сульфидов (пирит, серный колчедан) кислыми водами и восстановления сульфатов сульфатредуцирующими бактериями. Сероводород обладает резким неприятным запахом, вызывает коррозию металлических стенок труб, баков и котлов и является общеклеточным и каталитическим ядом. Соединяясь с железом образует черный осадок сернистого железа FeS. По этим причинам, а также вследствие интенсификации процессов коррозии, сероводород следует полностью удалять из воды хозяйственно-питьевого назначения (по ГОСТ 2874-82 "Вода питьевая"). СанПиН 2.1.4.559-96 (СанПиН2.1.4.1074-01) на питьевую воду мало того, что допускает присутствие сероводорода в воде до 0,03 мг/л, а сульфидов - до 3 мг/л, так эти цифры ещё никак не согласуется с элементарными знаниями химии: по данным диссоциации сероводорода и сульфидов в воде, при рН=9,0 (верхняя граница норматива на питьевую воду) доля сульфидов составляет примерно 98,5-99%, то есть в сто раз выше, чем сероводорода, и ПДК сульфидов соответственно должен быть не выше 0,3 мг/л . |
|
Микробиологические показатели |
Общая бактериальная загрязненность воды характеризуется количеством бактерий, содержащихся в 1 мл воды. Согласно ГОСТу, питьевая вода не должна содержать более 100 бактерий в 1 мл. Особую важность для санитарной оценки воды имеет определение бактерий группы кишечной палочки. Присутствие кишечной палочки свидетельствует о загрязнении воды фекальными стоками и, следовательно, о возможности попадания в нее болезнетворных бактерий, в частности бактерий брюшного тифа. В связи с тем, что при биологическом анализе воды определение патогенных бактерий затруднено, бактериологические определения сводятся к определению общего числа бактерий в 1 мл воды, растущих при 37"С, и кишечной палочки - бактерии коли. Наличие последней имеет индикаторные функции, т.е. свидетельствует о загрязнении воды выделениями людей и животных и т.п. Минимальный объем испытуемой воды, мл, приходящейся на одну кишечную палочку, называется колититром, а количество кишечных палочек в 1 л воды - коли-индексом. По ГОСТ 2874-82 допускается коли-индекс до 3, колититр - не менее 300, а общее число бактерий в 1 мл - до 100. По нормам СанПиН2.1.4.1074-01 допустимо общее микробное число 50 КОЕ/мл, общие колиформные бактерии КОЕ/100мл и термотолетарные колиформные бактерии КОЕ/100мл - не допускаются. |
|
Бактерии и вирусы |
из числа патогенных, т.е. паразитов, живущих на живом субстрате, развивающиеся в воде, могут вызвать заболевания брюшным тифом, амебиазом, парафитом, дизентерией, бруцеллезом, инфекционным гепатитом, острым гастроэнтеритом, сибирской язвой, холерой, полиомиелитом, туляремией, туберкулезом, диареей и др. Экспертами всемирной организации здравоохранения (ВОЗ) установлено, что 80% всех заболеваний в мире связано в той или иной степени связаны с неудовлетворительным качеством питьевой воды и нарушением санитарно-гигиенических и экологических норм водообеспечения. В связи с чем, проблема обеспечения высококачественной водой является актуальной. |
|
Влияние органических и неорганических веществ, бактерий и вирусов |
|
|
Название вещества, бактерии или вируса |
Органы и системы человека, на которые влияют эти соединения |
|
Неорганические вещества |
|
|
Бериллий |
Желудочно-кишечный тракт |
|
Кадмий |
Почки |
|
Медь |
Почки, печень |
|
Мышьяк |
Кожа, кровь; канцероген |
|
Нитраты и нитриты |
Мутации |
|
Ртуть |
Почки |
|
Свинец |
Почки, замедление развития |
|
Селен |
Кровь |
|
Таллий |
Желудочно-кишечный тракт, кровь, почки, печень |
|
Цианид |
Нервная система |
|
Органические вещества |
|
|
Бензол |
Канцерогены |
|
Пестициды (ДДТ, анахлор, гептахлор) |
Канцерогены |
|
Соединения хлора (винилхлорид, дихлорэтан) |
Кровь, почки, печень |
|
Фенол |
Печень, почки, обмен веществ |
|
Толуол |
Нервная система, почки, печень |
|
Бактерии и вирусы |
|
|
Кишечная палочка |
Желудочно-кишечный тракт |
|
Энтеровирусы |
Желудочно-кишечный тракт |
|
Вирус гепатита |
Печень |




